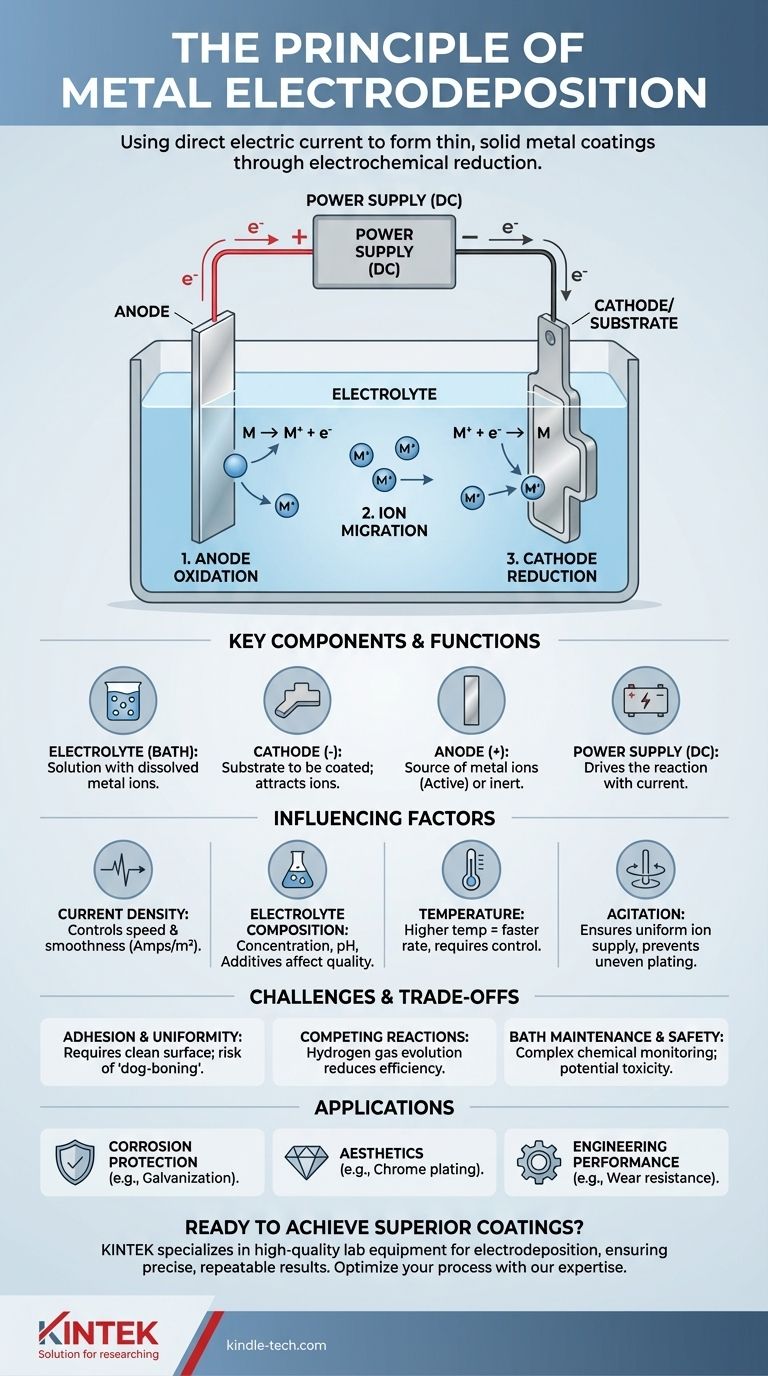
その核心において、電気めっきの原理とは、直流電流を使用して溶液中の溶解した金属イオンを還元し、導電性の物体上に薄い固体金属コーティングを形成するプロセスです。この制御された電気化学反応により、ある金属を別の金属の上に「めっき」することができ、母材の表面特性を根本的に変化させることができます。
プロセス全体は、電気分解回路の構築にかかっています。この回路では、電気が非自発的な化学反応を駆動し、液体浴中の正電荷を帯びた金属イオンに電子を受け取らせ、ターゲット表面上に中性の金属層として堆積させます。
電気めっきシステムの主要構成要素
原理を実際に応用して理解するには、まず電気分解セル内で連携して機能する4つの必須コンポーネントを理解する必要があります。
電解質(浴)
電解質は、めっきしたい金属イオンを高濃度で含む溶液です。これは通常、金属塩(硫酸銅や塩化ニッケルなど)を水に溶解させて作られます。浴には、最終的なコーティングの品質を制御するためのその他の添加剤も含まれています。
カソード(基材)
カソードはめっきしようとする物体です。電源の負極に接続されます。この負電荷が、電解質中の正電荷を帯びた金属イオンを引き寄せます。
アノード(金属源)
アノードは電源の正極に接続されます。これには2種類あります。
- 活動的アノード: めっきされる金属と同じ材料で作られています。ゆっくりと溶解し、カソード上に金属イオンが堆積するにつれて電解質中の金属イオンを補充します。
- 不活性アノード: 白金や炭素などの非反応性材料で作られています。溶解しませんが、電気回路を完成させる役割を果たします。この場合、浴中の金属イオンは時間とともに枯渇します。
電源
直流(DC)電源は、プロセス全体のエンジンとして機能します。これは、電子をカソードに送り込み、アノードから電子を引き抜くために必要な電位を提供し、めっき反応を強制的に発生させます。
電気化学的プロセス、ステップ・バイ・ステップ
堆積プロセスは、外部電源によって駆動される酸化と還元の連続的なループです。
ステップ1:アノードでの酸化
正のアノードでは、酸化反応が発生します。アノードが活動的である場合、その金属原子は電子を失い、正電荷を帯びたイオンになり、電解質に溶解します。これにより、金属イオンの供給が一定に保たれます。
ステップ2:電解質中のイオン移動
電解質中に存在する正電荷を帯びた金属イオン(陽イオン)は、溶液中を負電荷を帯びたカソードに向かって引き寄せられます。同時に、負イオン(陰イオン)は正のアノードに向かって移動し、溶液を電気的に中性に保ちます。
ステップ3:カソードでの還元
これが堆積ステップです。金属イオンがカソードに到達すると、電源から供給される電子を受け取ります。この還元反応により電荷が中和され、溶液から沈殿し、固体金属原子として表面に結合し、コーティング層が層をなして形成されます。
めっき品質に影響を与える主要な要因
最終的なコーティングの品質、厚さ、外観は自動的にもたらされるものではありません。これらは、いくつかの主要な変数の注意深い制御に依存します。
電流密度
これは、カソードの単位表面積あたりの電流量(A/m²で測定)です。
- 低い電流密度は、遅いものの、より滑らかで均一なコーティングをもたらす傾向があります。
- 高い電流密度はめっき速度を上げますが、適切に管理されないと、粗い、多孔質、または焼けた堆積物につながる可能性があります。
電解質の組成
金属イオン濃度、pHレベル、および添加剤(光沢剤やレベラーなど)の存在は、大きな影響を与えます。これらの添加剤は、堆積する金属の結晶構造を変化させ、その表面を鈍いものから鏡面光沢のあるものへと変化させます。
温度
浴の温度が高いほど、通常、電解質の導電率と堆積速度が増加します。ただし、過度に高い温度は望ましくない副反応や添加剤の分解を引き起こす可能性があります。
撹拌
浴をかき混ぜたり、何らかの方法で撹拌したりすることは極めて重要です。これにより、新鮮な金属イオンがカソード表面に供給され、特に複雑な形状での不均一なめっきを引き起こす局所的な枯渇を防ぎます。
トレードオフと課題の理解
電気めっきは強力ですが、一般的な失敗点を持つ精密なプロセスです。
コーティングの密着性と均一性
成功のための最も重要な単一の要因は基材の準備です。汚れた、または酸化された表面は密着性が悪くなり、コーティングが剥がれたり剥離したりする原因となります。さらに、電流は自然に鋭いエッジや角に集中するため、それらの部分でより厚い堆積物となり、凹部ではより薄い堆積物となる傾向があります。これは「ドッグボーン効果」として知られる問題です。
競合反応
主要な競合反応、特に水性電解質では、カソードでの水素ガスの生成を目的とした水の還元です。このプロセスは、金属堆積に通常使用される電流を消費し、全体の効率を低下させます。場合によっては、吸収された水素が基材を脆くすることもあります。
浴の維持管理と安全性
電気めっき浴は複雑な化学システムであり、pH、温度、化学濃度の絶え間ない監視と調整が必要です。シアン化物や六価クロムを含む多くの工業用めっき溶液は非常に毒性が高く、環境および作業者の安全に重大なリスクをもたらします。
用途に合わせた適切な選択を行う
コアとなる原理を理解することで、特定の目的に合わせてプロセスを調整できます。
- 腐食防止が主な焦点の場合: 目的は、亜鉛などの犠牲金属を鋼鉄上にめっきすること(亜鉛めっき)や、金などの貴金属による、高密度で非多孔質の層です。
- 美観が主な焦点の場合: クロムめっきやニッケルめっきで見られるように、滑らかで反射性のある表面を実現するには、電流密度を注意深く制御し、光沢剤などの特定の添加剤を使用する必要があります。
- 工学的性能(例:耐摩耗性)が主な焦点の場合: 硬質クロムめっきや無電解ニッケルコーティングなど、厚さと硬度の正確な制御が必要です。これらは、強力な密着性が不可欠な場合によく達成されます。
イオンと電子の流れを制御することにより、特定の工学的または美的なニーズを満たすように材料の表面を変換できます。

要約表:
| 主要コンポーネント | 電気めっきにおける役割 |
|---|---|
| 電解質(浴) | 堆積される溶解金属イオンを含む溶液。 |
| カソード(基材) | めっきされる物体。正の金属イオンを引き寄せる。 |
| アノード(金属源) | 金属イオンの供給源(活動的)または不活性電極。 |
| 電源(DC) | 非自発的な反応を駆動するための電流を供給する。 |
| 電流密度 | 堆積速度とコーティング品質(平滑性)を制御する。 |
| 浴添加剤 | 最終的なコーティング特性(例:光沢、硬度)に影響を与える。 |
ラボで優れた金属コーティングを実現する準備はできましたか?
電気めっきの原理を理解することは第一歩です。それを効果的に実装するには、適切な機器と消耗品が必要です。KINTEKは、電気めっきおよびその他の表面工学プロセスのための高品質なラボ機器を専門としており、正確で信頼性が高く、再現性のある結果を達成できるよう支援します。
研究、品質管理、または新しいコーティングの開発に重点を置いているかどうかにかかわらず、当社の専門知識がお客様のラボのニーズをサポートできます。
当社の専門家チームに今すぐお問い合わせいただき、電気めっきプロセスの最適化をどのように支援できるかご相談ください!
ビジュアルガイド