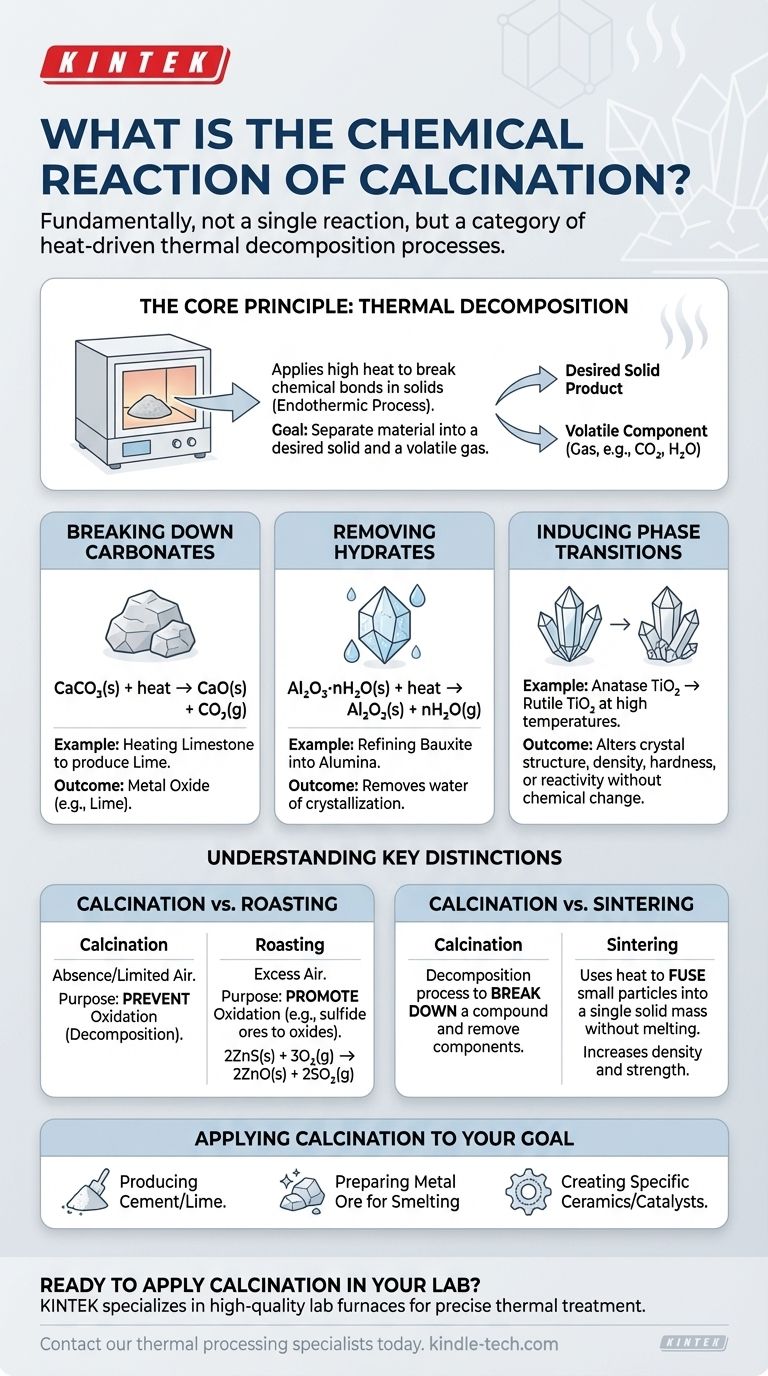
根本的に、焼成は単一の化学反応ではなく、特定の成果(熱分解)によって定義される一連の熱駆動プロセスです。多くの反応がこの範疇に含まれますが、最も一般的な例は、石灰石(炭酸カルシウム)を加熱して生石灰(酸化カルシウム)と二酸化炭素ガスを生成するような、炭酸塩の分解です。
焼成は、制御された雰囲気中で高温を使用して材料を分解する熱処理プロセスです。その主な目的は、二酸化炭素や水などの揮発性成分を追い出し、残った固体の化学的および物理的特性を精製または変化させることです。
核心原理:熱分解
焼成は、固体に化学結合を破壊するのに十分な熱エネルギーを加えることによって機能します。このプロセスは常に吸熱的であり、進行するためにはエネルギー(熱)の投入が必要です。目標は、材料を目的の固体生成物と、ガスとして追い出すことができる揮発性成分に分離することです。
炭酸塩の分解
これは焼成の古典的かつ最も広範な応用例であり、特にセメントの製造において顕著です。金属炭酸塩を加熱すると、金属酸化物と二酸化炭素ガスに分解します。
石灰石の場合、反応は次のとおりです。
CaCO₃(s) + heat → CaO(s) + CO₂(g)
ここでは、固体炭酸カルシウムが固体酸化カルシウム(生石灰)と気体二酸化炭素に分解します。
結晶水(水和物)の除去
多くの鉱物は水和物として存在します。つまり、水分子が結晶構造に取り込まれています。焼成は、この水を追い出すために使用されます。このプロセスは「乾燥」と呼ばれることもありますが、化学的分解です。
例えば、ボーキサイト鉱石をアルミナに精製するには、水和酸化アルミニウムを焼成する必要があります。
Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g)
この工程で水が除去され、酸化アルミニウムが濃縮されます。これはアルミニウム金属を製造するために必要な前駆体です。
相転移の誘発
あまり一般的ではありませんが、焼成は、熱が分解を引き起こすのではなく、材料の結晶構造(相)を変化させるプロセスを指すことがあります。これにより、化学式を変えることなく、密度、硬度、反応性などの物理的特性が変化します。
一例として、二酸化チタン(TiO₂)の一形態であるアナターゼを高温でより安定なルチル相に変換することが挙げられます。

重要な区別を理解する
焼成の価値は、他の一般的な熱処理プロセスと比較することでより明確になります。特定の条件、特に雰囲気は、結果を決定します。
焼成と焙焼の比較
これが最も重要な区別です。焼成は、意図的に酸化を防ぐために、空気の不在下または限られた供給下で行われます。
対照的に、焙焼は、酸化を促進するために、過剰な空気中で行われます。通常、硫化物鉱石に適用され、酸化物に変換されます。例えば、硫化亜鉛の焙焼:
2ZnS(s) + 3O₂(g) → 2ZnO(s) + 2SO₂(g)
焼成と焼結の比較
これらのプロセスは反対の目的を持っています。焼成は、化合物を分解し、成分を除去するために使用される分解プロセスです。
一方、焼結は、熱(融点未満)を使用して微粒子を単一の固体塊に融合させます。密度と強度を高め、材料を溶かすことなく本質的に「溶接」します。
焼成をあなたの目的に適用する
あなたが気にする特定の焼成反応は、出発材料と目的の最終製品に完全に依存します。
- セメントまたは生石灰の製造が主な焦点の場合: 炭酸カルシウムを反応性の高い酸化カルシウムに分解するために焼成を使用しています。
- 製錬のために金属鉱石を準備することが主な焦点の場合: 金属含有量を濃縮するために、水(水和物から)または二酸化炭素(炭酸塩から)を除去するために焼成を使用している可能性が高いです。
- 特定のセラミックや触媒を作成することが主な焦点の場合: アルミナやチタニアなどの材料で目的の結晶相と表面積を得るために焼成を使用している可能性があります。
結局のところ、焼成は、原材料をより有用で、濃縮され、または反応性の高い形態に変換するための材料科学における基本的なツールです。
要約表:
| 焼成反応の種類 | 反応例 | 主な成果 |
|---|---|---|
| 炭酸塩の分解 | CaCO₃(s) + heat → CaO(s) + CO₂(g) |
金属酸化物(例:生石灰)を生成する |
| 水和物の分解 | Al₂O₃·nH₂O(s) + heat → Al₂O₃(s) + nH₂O(g) |
結晶水を除去する |
| 相転移 | アナターゼ TiO₂ → ルチル TiO₂ | 結晶構造と特性を変化させる |
あなたの研究室で焼成を適用する準備はできましたか?
新しい触媒の開発、鉱石の処理、高度なセラミックスの合成のいずれであっても、正確な熱処理が不可欠です。KINTEKは、信頼性の高い焼成プロセス向けに設計された高品質のラボ用電気炉と装置を専門としています。
私たちは、均一な加熱、正確な温度制御、一貫した結果を得るために必要なツールを提供します。当社の専門家が、お客様固有の材料と用途に最適な装置の選択をお手伝いします。
当社の熱処理スペシャリストに今すぐお問い合わせいただき、プロジェクトの要件についてご相談の上、KINTEKがお客様の研究開発をどのように強化できるかをご確認ください。
ビジュアルガイド
関連製品
- 電気ロータリーキルン熱分解炉プラントマシンカルサイナー小型ロータリーキルン回転炉
- 電気ロータリーキルン連続稼働小型ロータリー炉加熱熱分解プラント
- 垂直高温石墨真空石墨化炉
- 黒鉛真空炉 高熱伝導率フィルム黒鉛化炉
- 超高温黒鉛真空黒鉛化炉



















