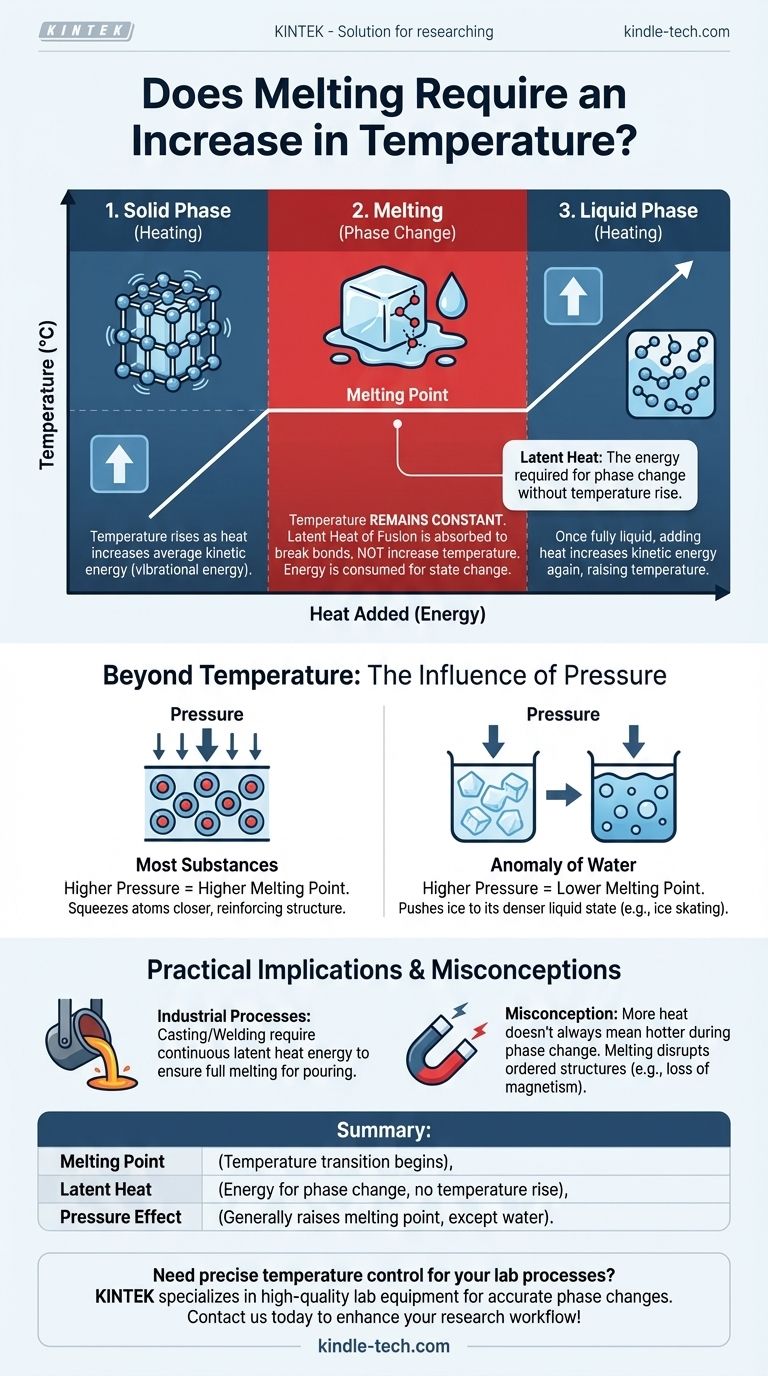
熱、温度、融解の関係は誤解されがちです。 固体が融解するためには、熱の形でエネルギーを加える必要があります。このプロセスは、まず物質の温度を特定の融点に達するまで上昇させます。しかし、固体から液体への実際の変化の間、より多くの熱が供給されていても、温度は一定に保たれます。
物質はまず融点まで加熱される必要がありますが、融解プロセス自体は一定温度で起こります。加えられるエネルギーは潜熱として知られ、物質の全体的な温度を上昇させるためではなく、固体の構造の結合を破壊するために使用されます。
相変化の物理学
融解がなぜ一定温度で起こるのかを理解するためには、まず熱と温度を区別する必要があります。これらは関連していますが、同じではありません。
温度とは?
温度は、物質内の原子または分子の平均運動エネルギーの尺度です。固体では、これらの原子は結晶格子のような固定構造に固定されていますが、絶えず振動しています。熱を加えると、この振動エネルギーが増加し、それが温度の上昇として測定されます。
融点への到達
熱を加え続けると、原子の振動はますます激しくなります。最終的に、振動が固定位置に原子を保持している剛性の結合を破壊するのに十分な強さになるエネルギーレベルに達します。この特定の温度が融点です。
潜熱の役割
融点では、重要な変化が起こります。供給される追加の熱エネルギー(融解潜熱として知られる)は、今や残りの固体の構造の結合を破壊するためだけに費やされます。それは分子の振動を速くするために使われるのではありません。
エネルギーが物質の運動エネルギーを増加させるためではなく、物質の状態(固体から液体へ)を変化させるために消費されるため、すべての固体が液体になるまで、温度は完全に一定に保たれます。
液体状態
固体がすべて融解すると、物質は完全に液体状態になります。この時点から、さらに加える熱は再び分子の運動エネルギーを増加させ、液体の温度を上昇させます。

温度を超えて:圧力の影響
温度は融解を決定する唯一の要因ではありません。圧力は重要で、時には直感に反する役割を果たします。
圧力が融解にどのように影響するか
ほとんどの物質では、外部圧力を上げると融点が上昇します。高圧は原子を物理的に押し付け、固体構造を強化します。これは、物質が融解するために、より多くのエネルギー(したがってより高い温度)が必要であることを意味します。
水の例外性
水は注目すべき例外です。水の固体形態(氷)は、液体形態よりも密度が低いです。氷に圧力をかけると、より密度の高い状態である液体水に押しやられます。これは、高圧下では、氷が標準の融点である0℃(32°F)よりも低い温度で融解できることを意味します。この原理は、アイススケートの刃が氷の上を滑る方法に寄与しています。
実際的な意味と誤解
このプロセスを理解することは学術的なものではなく、科学および工学において直接的な結果をもたらします。
誤解:熱が多ければ常に熱くなる
最も一般的な誤解は、継続的に熱を加えても常に何かが熱くなるということです。融解や沸騰などの相変化の間、これは正しくありません。エネルギー投入は、物質の温度を上げるのではなく、その状態を変化させるという仕事を行っています。
実用上なぜ重要か
金属の鋳造や溶接などの産業プロセスにおいて、この原理は極めて重要です。炉は、金属を融点に到達させるだけでなく、全質量が注湯のために完全に液体になることを保証するために、かなりの継続的な追加エネルギー(潜熱)を供給する必要があります。同様に、融解は物質の秩序だった原子構造を破壊します。これが、磁化された鋼片をある点(そのキュリー温度、融点とは異なるが関連している)を超えて加熱すると、整然とした磁区が破壊されるため、磁性を失う理由です。
目的のための正しい選択をする
あなたの応用が、このプロセスのどの部分があなたにとって最も重要かを決定します。
- 基本的な物理学の理解が主な焦点である場合: 相変化の間、温度は一定であり、加えられるエネルギーは潜熱と呼ばれ、状態を変えるために使用されることを覚えておいてください。
- 材料科学または工学が主な焦点である場合: 物質を完全に融解させるには、融点に達した後でも、正確で継続的なエネルギー投入が必要であることを認識してください。
- 環境への影響を考慮している場合: 圧力は物質の融点を大幅に変更する可能性があり、ほとんどの材料では融点を上昇させますが、水のような重要な例外では低下させることに注意してください。
温度と熱エネルギーのこの区別を理解することは、あらゆる物質の挙動を制御し予測するための基本です。
要約表:
| 概念 | 説明 |
|---|---|
| 融点 | 固体が液体への移行を開始する温度。 |
| 融解潜熱 | 温度変化なしに融解中に吸収されるエネルギー。 |
| 圧力効果 | 高圧は融点を上昇させる(水の場合は低下させる)。 |
| 実用的な応用 | 金属鋳造や溶接などの産業プロセスにとって極めて重要。 |
実験室プロセスで正確な温度制御が必要ですか? KINTEKは、融解などの相変化を正確に処理できるように設計された炉や加熱システムを含む、高品質の実験装置を専門としています。金属、ポリマー、その他の材料を扱う場合でも、当社のソリューションは効率的なエネルギー管理と一貫した結果を保証します。当社の実験装置が研究や生産ワークフローをどのように強化できるかを探るために、今すぐお問い合わせください!
ビジュアルガイド