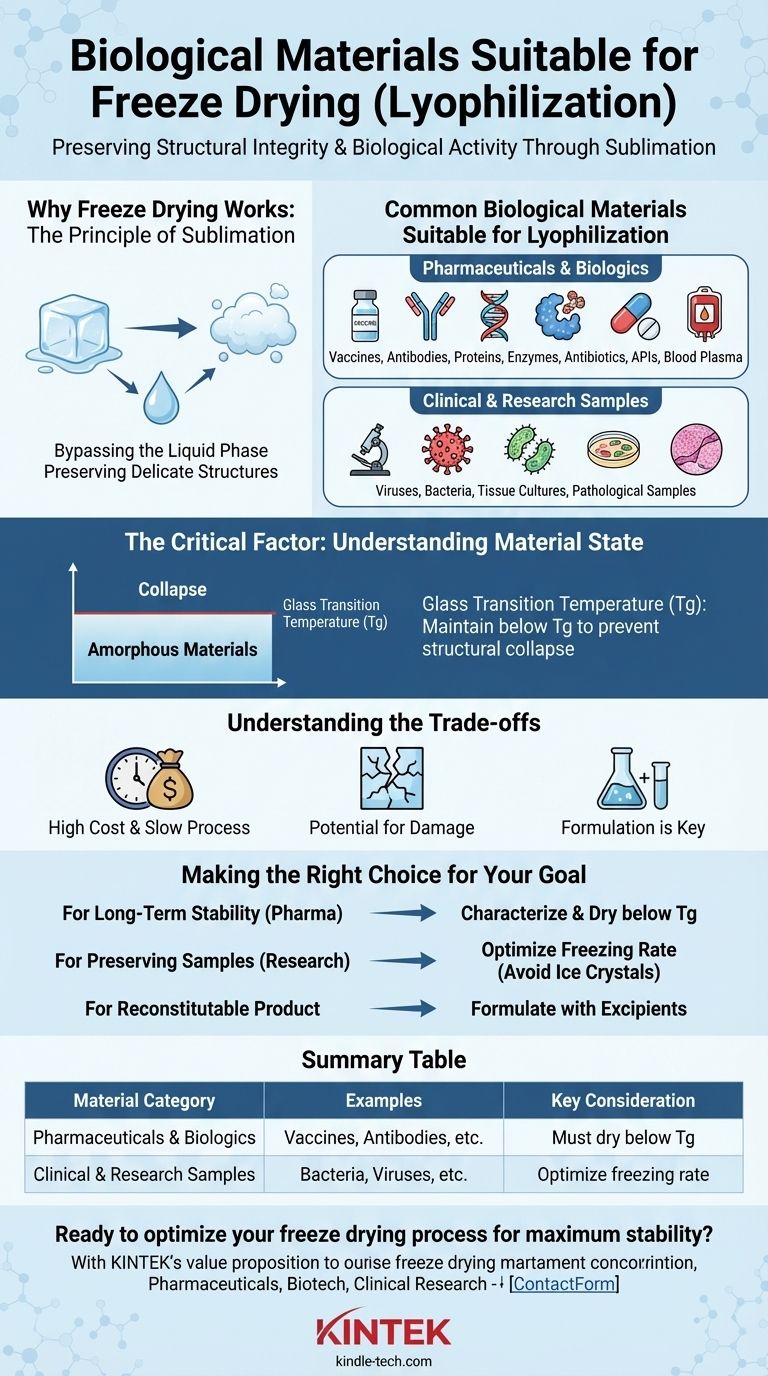
幅広い生物学的材料が、技術的には凍結乾燥(ライオフィリゼーション)として知られるフリーズドライに適しています。これには、ワクチン、抗体、タンパク質、酵素などのデリケートな製品や、血漿、細菌、組織培養などの臨床検体が含まれます。保存を成功させる鍵は、材料そのものだけでなく、分子レベルでの材料の構造的完全性を維持するためにプロセスを制御することにあります。
生物学的材料がフリーズドライに適しているかどうかは、それが「何か」であるかよりも、安定した固体状の「ガラス状」の状態を形成できるかどうかにかかっています。目標は、乾燥プロセス中に材料を臨界温度以下に保ち、構造の崩壊を防ぎ、その活性を維持することです。

フリーズドライが機能する理由:昇華の原理
フリーズドライは、水による損傷を最小限に抑えるため、デリケートな生物学的材料を保存するためのゴールドスタンダードです。
液相の回避
このプロセスには、まず材料を凍結し、次に深い真空下に置くことが含まれます。これにより、凍結した水が昇華と呼ばれるプロセスで固体(氷)から直接気体(水蒸気)に変化します。
液相を完全に回避することにより、昇華はタンパク質の変性や細胞の破裂を引き起こす表面張力の破壊的な力を回避します。
デリケートな構造の保存
液体の水がないため、タンパク質、酵素、その他の高分子の複雑な三次元構造が固定されます。これにより、生物学的活性が維持され、デリケートな医薬品や研究材料にとって理想的なプロセスとなります。
ライオフィリゼーションに適した一般的な生物学的材料
リストは広範ですが、適切な材料は通常、用途に基づいて2つの主要なカテゴリに分類されます。
医薬品とバイオロジクス
これは最も一般的な用途であり、安定性と長い保存期間が最も重要です。
- ワクチンと抗体: ライオフィリゼーションにより、注射前に再構成できる安定した輸送しやすい粉末が作成されます。
- タンパク質、ペプチド、酵素: これらの大きく壊れやすい分子は、活性を維持したまま保存されます。
- 抗生物質とAPI: 多くの原薬(API)は、保管と輸送のために安定化されます。
- 血漿: 血漿から水分を除去することで、冷蔵なしでの長期保存が可能になります。
臨床および研究サンプル
フリーズドライは、後で分析または使用するために検体を安定化するためにも使用されます。
- ウイルスと細菌: 研究またはプロバイオティクス用途のために、培養物が休眠状態で保存されます。
- 病理学的サンプル: 組織やその他の病理学的検体は、構造的な歪みなく組織学的または分析的研究のために乾燥されます。
決定的な要因:材料の状態の理解
フリーズドライの成功は、凍結した材料の物理的な状態を理解することにかかっています。ほとんどの生物学的製剤は単純な結晶構造ではありません。
非晶質材料
ほとんどの生物学的製品は非晶質であり、これは凍結時に整った結晶構造を形成しない多成分混合物であることを意味します。代わりに、粘性のあるガラス状の状態に固化します。
ガラス転移温度(Tg)の重要性
これらの非晶質材料にとって最も重要なパラメータは、ガラス転移温度(Tg)です。これは、材料が固体で安定した「ガラス状」の状態にある温度以下の温度です。
一次乾燥フェーズ中の温度がTgを超えると、材料は軟化して流れ、崩壊として知られる構造の損失を引き起こします。これは製品を台無しにし、その外観、安定性、生物学的活性を損ないます。したがって、昇華プロセス全体はこの臨界温度以下で行われる必要があります。
トレードオフの理解
ライオフィリゼーションは強力ですが、完璧または普遍的な解決策ではありません。考慮しなければならない明確なトレードオフが伴います。
高いコストと遅いプロセス
フリーズドライヤーは高価な設備であり、プロセス自体が非常に遅く、数日かかることがよくあります。これにより、最もエネルギーを消費し、時間のかかる保存方法の1つになります。
損傷の可能性
特定の製品に合わせてプロセスが慎重に最適化されていない場合でも、損傷が発生する可能性があります。凍結速度が遅すぎると、大きな氷晶が細胞構造を損傷する可能性があり、不適切な真空または温度制御は製品の崩壊につながる可能性があります。
製剤が鍵
多くの材料は単独ではフリーズドライできません。ガラス転移温度を上げ、乾燥中および保管中に分子を保護するために、糖類やポリマーなどの賦形剤(安定化剤)の添加が必要です。
目標に応じた適切な選択
フリーズドライへのアプローチは、材料の最終的な目的に応じて決定されるべきです。
- 長期的な医薬品の安定性を最優先する場合: 製剤のガラス転移温度(Tg)を正確に特性評価し、その温度より十分に低い温度で乾燥を実行する必要があります。
- 分析のために組織や培養物を保存することを最優先する場合: 氷晶の大きな形成によるサンプルの構造への物理的損傷を防ぐために、初期凍結速度の最適化が重要です。
- 再構成可能な製品の作成を最優先する場合: 最終的な乾燥「ケーキ」が安定し、容易に溶解するように、適切な賦形剤で製剤化することが不可欠です。
結局のところ、フリーズドライを成功させることは、最初から最後まで材料が安定した固体状態に留まることを保証する制御の科学です。
要約表:
| 材料カテゴリー | 例 | 重要な考慮事項 |
|---|---|---|
| 医薬品とバイオロジクス | ワクチン、抗体、タンパク質、酵素、血漿 | 崩壊を防ぐためにガラス転移温度(Tg)以下で乾燥させる必要がある |
| 臨床および研究サンプル | 細菌、ウイルス、組織培養、病理学的検体 | 氷晶による損傷を防ぐために凍結速度を最適化する |
最大の安定性のためにフリーズドライプロセスを最適化する準備はできましたか?
KINTEKでは、正確なライオフィリゼーションに合わせた高品質のラボ機器と消耗品の提供を専門としています。デリケートな医薬品、臨床検体、研究材料を保存する場合でも、当社のソリューションは構造的完全性と生物学的活性の維持を保証します。
当社がお手伝いすること:
- 特定の生物学的材料に最適な機器の選択。
- ガラス転移温度(Tg)などの重要なパラメータの理解。
- 長期的な安定性を備えた一貫性のある信頼性の高い結果の達成。
製薬、バイオテクノロジー、臨床研究の研究所を対象としており、KINTEKはすべてのフリーズドライのニーズに対応するパートナーです。フリーズドライの目標達成を支援する方法について、今すぐお問い合わせください!
ビジュアルガイド