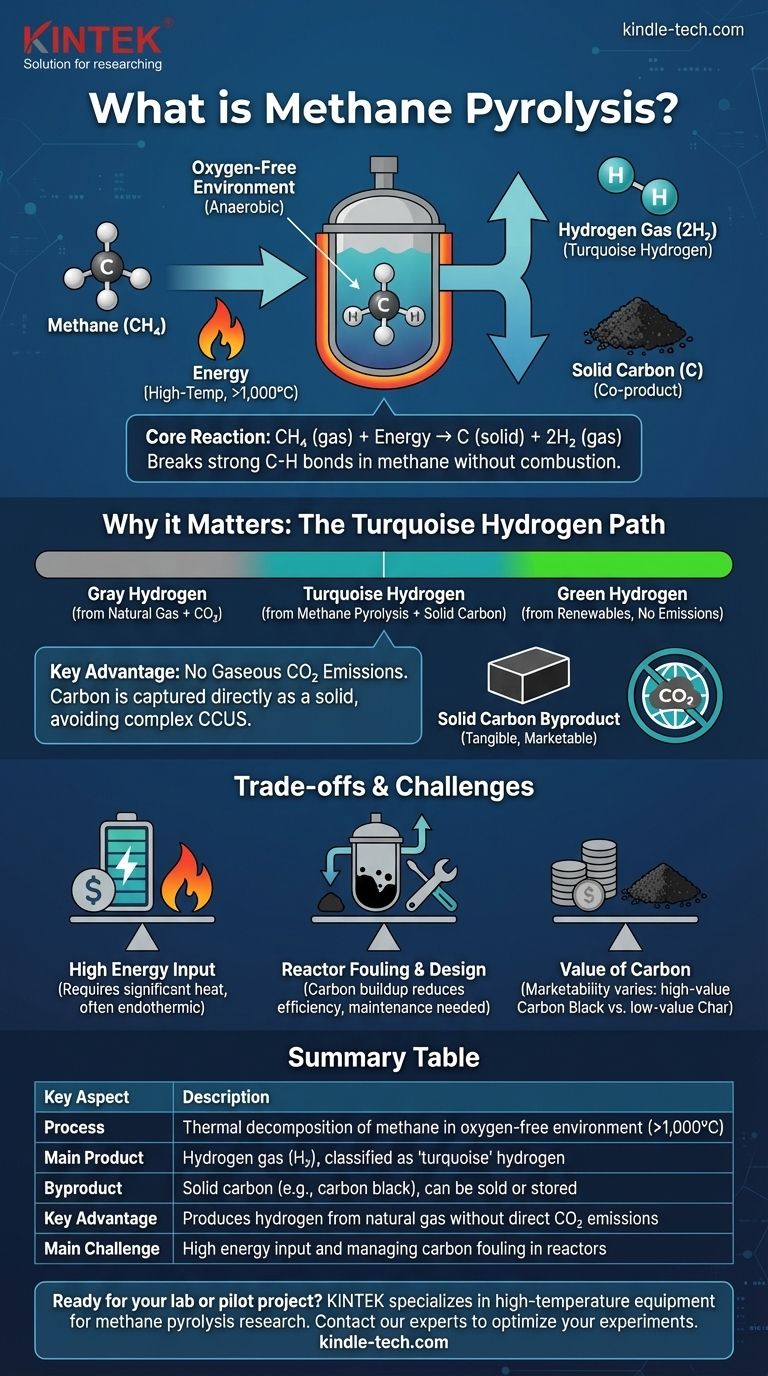
最も簡単に言えば、メタン熱分解は、メタン(CH₄)をその基本的な構成要素である水素ガス(H₂)と固体炭素(C)に分解する化学プロセスです。これは、酸素のない環境でメタンを非常に高い温度に加熱することによって達成されます。この酸素の不在は極めて重要です。なぜなら、メタンが燃焼するのを防ぎ、代わりに分解を強制するからです。
メタン熱分解は単なる化学反応ではなく、二酸化炭素を大気中に放出することなく天然ガスから価値ある水素を生産するための戦略です。炭素は固体で管理しやすい形で回収され、化石燃料からの水素製造の排出プロファイルを根本的に変えます。
主要な化学反応
メタン熱分解の巧妙さは、その直接性にあります。メタン分解またはメタン分解とも呼ばれるこのプロセスは、有機化学において最も強力な単結合の1つを破るために熱エネルギーに依存しています。
基本方程式
この反応は、シンプルでクリーンな方程式によって支配されます:CH₄(ガス)+ エネルギー → C(固体)+ 2H₂(ガス)。メタン分子1分子から、固体炭素原子1つと水素ガス分子2つが得られます。
高温の役割
メタン中の安定した炭素-水素結合を切断するには、かなりのエネルギー投入が必要であり、このプロセスを吸熱性にします。これは通常、メタンを1,000°C(1,832°F)以上に加熱することによって達成されますが、触媒によってこの要件が緩和されることもあります。
酸素の不在
プロセス全体は、嫌気性(酸素フリー)環境で発生しなければなりません。酸素が存在すると、メタンは燃焼し、目的の水素と固体炭素の代わりに二酸化炭素(CO₂)と水(H₂O)を生成します。

なぜ熱分解が水素製造にとって重要なのか
メタン熱分解は、エネルギー転換における潜在的な架け橋技術として大きな注目を集めています。これは、他の確立された水素製造方法と比較して独自の付加価値を提供します。
「ターコイズ」水素経路
水素は、その製造方法によって色分けされることがよくあります。グレー水素は、大量のCO₂を排出するプロセスである水蒸気メタン改質(SMR)を介して天然ガスから製造されます。グリーン水素は、再生可能エネルギーを使用した電気分解によって製造され、排出量はゼロです。
メタン熱分解は、ターコイズ水素として知られるものを作り出します。化石燃料を原料(メタン)として使用しますが、気体状の炭素排出物を生成しないため、炭素強度スペクトル上でグレーとグリーンの間に位置します。
主要な利点:気体状炭素排出物がないこと
熱分解の決定的な利点は、炭素が直接固体として捕捉されることです。これにより、グレー水素を低排出の「ブルー」水素に変換するために必要となる、複雑で高価な炭素回収・利用・貯留(CCUS)システムが不要になります。
固体炭素の副産物
CO₂が管理すべき廃棄物となる他のプロセスとは異なり、熱分解からの固体炭素は具体的な副産物です。その形態、純度、市場価値は、プロセスの全体的な経済性に不可欠です。
トレードオフと課題の理解
有望である一方で、メタン熱分解は万能薬ではありません。その実現可能性は、重大な技術的および経済的な課題を解決できるかどうかにかかっています。
高いエネルギー投入量
吸熱プロセスであるため、熱分解には大量の連続的な高温熱供給が必要です。このエネルギー源がどこから来るのかが重要な要素となります。もし熱がより多くの天然ガスを燃焼させることによって生成される場合、プロセスの全体的な炭素排出量は増加し、「低炭素」としての資格が損なわれます。プラズマ加熱や抵抗加熱に再生可能電力を利用することは解決策ですが、コストが増加します。
反応器の設計とファウリング
極端な温度でプロセスを管理することは、大きなエンジニアリング上の課題です。主な問題は炭素ファウリングであり、固体炭素の副産物が反応器の表面、触媒、熱交換器に堆積し、効率を低下させ、定期的なシャットダウンと清掃が必要になります。
炭素の価値
ターコイズ水素の経済的実現可能性は、多くの場合、固体炭素の副産物を販売できるかどうかにかかっています。この炭素の価値は、タイヤや顔料に使用される高価値のカーボンブラックから、処分費用がかかる可能性のある低価値の炭素チャールまたはすすまで、劇的に異なります。一貫した高純度の炭素製品を生産することが、主要な技術的目標です。
目標に合わせた適切な選択
メタン熱分解技術の評価は、お客様固有の戦略的目標と一致している必要があります。
- 既存の天然ガスインフラの脱炭素化が主な焦点である場合:熱分解は、直接的なCO₂排出なしに水素を製造するための説得力のある経路を提供し、CCUSの資本コストと地質学的リスクを回避しながら、既存のガスパイプラインを活用できる可能性があります。
- 絶対的に最もクリーンな水素の製造が主な焦点である場合:専用の再生可能エネルギーで駆動される電気分解によって製造されるグリーン水素は、化石燃料の使用を完全に排除するため、依然としてゴールドスタンダードです。
- 経済的実現可能性が主な焦点である場合:熱分解プロジェクトの成功は、安価な天然ガスへのアクセス、熱源としての低コストかつ低炭素のエネルギー源、および製造される高価値の固体炭素の確実な市場という3つの要因によって決まります。
メタン熱分解は、脱炭素化のための強力かつ複雑なツールであり、水素そのものを製造するのと同じくらい、エネルギー投入量と炭素排出量を管理することが重要です。
要約表:
| 主要な側面 | 説明 |
|---|---|
| プロセス | 酸素のない環境下でのメタンの熱分解(1,000°C超)。 |
| 主要生成物 | 水素ガス(H₂)、「ターコイズ」水素として分類される。 |
| 副産物 | 固体炭素(例:カーボンブラック)。販売または貯蔵が可能。 |
| 主な利点 | 天然ガスから直接CO₂を排出せずに水素を製造する。 |
| 主な課題 | 高いエネルギー投入量と反応器内での炭素ファウリングの管理。 |
研究室またはパイロットプロジェクト向けの水素製造ソリューションの検討準備はできましたか? KINTEKは、メタン熱分解などのプロセスの研究開発に不可欠な高温実験装置と消耗品の専門家です。反応器、発熱体、分析ツールが必要な場合でも、当社の専門知識が実験の最適化と技術のスケールアップを支援します。クリーンエネルギーの革新をどのようにサポートできるかについて、当社の専門家にご相談ください。今すぐお問い合わせください。
ビジュアルガイド
関連製品
- 電気ロータリーキルン小型ロータリー炉バイオマス熱分解プラント
- 電気ロータリーキルン連続稼働小型ロータリー炉加熱熱分解プラント
- 電気ロータリーキルン熱分解炉プラントマシンカルサイナー小型ロータリーキルン回転炉
- 多様な科学的用途に対応するカスタマイズ可能な実験室用高温高圧リアクター
- ラボ用小型ステンレス高圧オートクレーブリアクター











