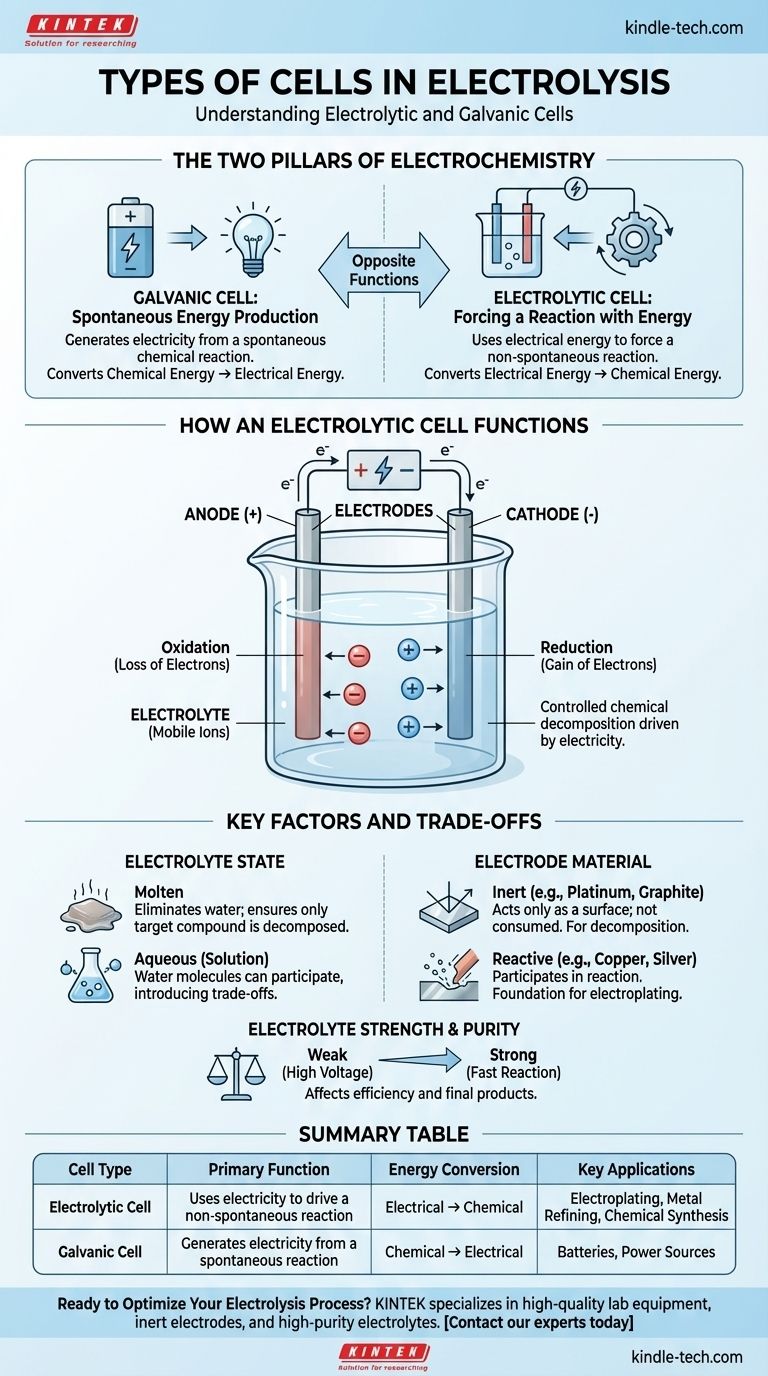
その核心において、電気分解は電解セルとして知られる特定の種類の電気化学セル内で起こります。このセルは、電気化学セルの2つの基本的なタイプのうちの1つであり、もう1つはガルバニセルです。電解セルは、電気エネルギーを使用して非自発的な化学反応を強制的に起こさせますが、ガルバニセルはその逆で、自発的な化学反応から電気を生成します。
決定的な違いは目的です。ガルバニセル(電池のようなもの)は化学反応から電気を生成します。電解セルは、それ自体では起こらない化学反応を駆動するために電気を使用します。
電気化学の二つの柱
電気分解に使用されるセルを理解するには、まずその対となるものを理解する必要があります。どちらのセルタイプも電気化学の基礎ですが、それぞれ異なる機能を果たします。
ガルバニセル:自発的なエネルギー生成
ガルバニセルは、一般的に電池として知られているものです。これは、自然に起こりたがる自発的な化学反応を利用します。
この反応が進行すると、電流の形でエネルギーが放出されます。これは、貯蔵された化学エネルギーを電気エネルギーに直接変換します。
電解セル:エネルギーで反応を強制する
電解セルは電気分解の原動力です。外部エネルギーを供給することで、非自発的な化学反応を起こさせるように設計されています。
外部電源(電源装置など)からセルに電流を供給します。これにより、物質の分解が強制され、新しい物質を生成することで電気エネルギーを化学エネルギーに効果的に変換します。

電解セルの機能
電気分解のプロセスは、電気によって駆動される制御された化学分解です。これには、いくつかの主要な構成要素が連携して機能する必要があります。
主要な構成要素
電解セルは、電極(陽極と陰極)が電解質に浸されている状態で構成されます。外部電源がこれらの電極に接続され、回路を形成します。
電解質の役割
電解質は分解される物質です。通常、溶融状態または溶液(水溶液)に溶解したイオン化合物です。
この物質には、自由に移動して電荷を運ぶことができる移動性イオンが含まれている必要があります。電解質は一般的に酸、塩基、または塩の溶液です。
電極の機能
電極は、電気が電解質に出入りする導体です。
- 陽極:正極。負イオン(アニオン)を引き付け、そこで酸化(電子の喪失)が起こります。
- 陰極:負極。正イオン(カチオン)を引き付け、そこで還元(電子の獲得)が起こります。
外部電源は、この電荷分離を維持し、プロセス全体を駆動するものです。
主要な要因とトレードオフの理解
電気分解の結果は自動ではありません。生成される特定の生成物は、選択した材料と条件に完全に依存します。
電解質の状態:溶融 vs. 水溶液
電解質の状態は重要な決定事項です。水溶液(水に溶解)を使用する場合、水分子自体が反応に参加する可能性があります。
これによりトレードオフが生じます。反応の駆動しやすさによっては、溶解した化合物ではなく水が分解される可能性があります。溶融電解質を使用すると、方程式から水が排除され、目的の化合物のみが分解されます。
電極材料:不活性 vs. 反応性
電極は、反応において受動的な参加者であることも、能動的な役割を果たすこともあります。
- 不活性電極(例:白金、グラファイト):これらは反応が起こる表面としてのみ機能します。消費されることはなく、電解質自体を分解したい場合、例えば水を水素と酸素に分解する場合に使用されます。
- 反応性電極(例:銅、銀):これらは溶解したり、化学反応に参加したりすることがあります。これは電気めっきの原理であり、陽極が溶解し、その金属イオンが陰極の物体に堆積します。
電解質の強度と純度
電気分解の効率は電解質にも影響されます。完全にイオンに解離する強電解質は、電気をよく伝導し、より速い反応を可能にします。
弱電解質は、反応を開始および維持するためにより多くのエネルギー(より高い電圧)を必要とします。電解質中に他の酸化剤または還元剤が存在すると、最終生成物が変化することもあります。
これをあなたの目標に適用する
電解セルの機能を理解することで、特定の産業的および科学的目的のために化学反応を制御することができます。
- 純粋な物質の生産が主な焦点である場合:不活性電極と高純度電解質(溶融または水溶液)を選択して、目的の化合物を分解するようにします。これは、ボーキサイト鉱石からアルミニウムを生産する場合などです。
- 金属をコーティングまたは精製することが主な焦点である場合:コーティング材料で作られた反応性陽極と、その同じ金属のイオンを含む電解質を使用します。これは電気めっきと電解精錬の基礎です。
- 電気を生成することが主な焦点である場合:自発的な反応からエネルギーを放出するのがその機能であるため、電解セルではなくガルバニセルが必要です。
最終的に、電気分解は電気エネルギーを使用して化学変化を正確に制御し、駆動するための強力な方法を提供します。
まとめ表:
| セルタイプ | 主な機能 | エネルギー変換 | 主な用途 |
|---|---|---|---|
| 電解セル | 電気を使用して非自発的な反応を駆動する | 電気 → 化学 | 電気めっき、金属精錬、化学合成 |
| ガルバニセル | 自発的な反応から電気を生成する | 化学 → 電気 | 電池、電源 |
電気分解プロセスを最適化する準備はできていますか?
適切なセルタイプと構成要素を理解することは、効率的な電気めっき、金属精錬、または化学合成にとって非常に重要です。KINTEKは、不活性電極や高純度電解質を含む高品質の実験装置と消耗品を提供することに特化しており、お客様の電気分解プロセスが正確かつ効果的であることを保証します。
お客様の特定の用途についてご相談いただくには、今すぐ当社の専門家にお問い合わせください。当社のソリューションがお客様のラボの能力と結果をどのように向上させることができるかをご確認ください。
ビジュアルガイド