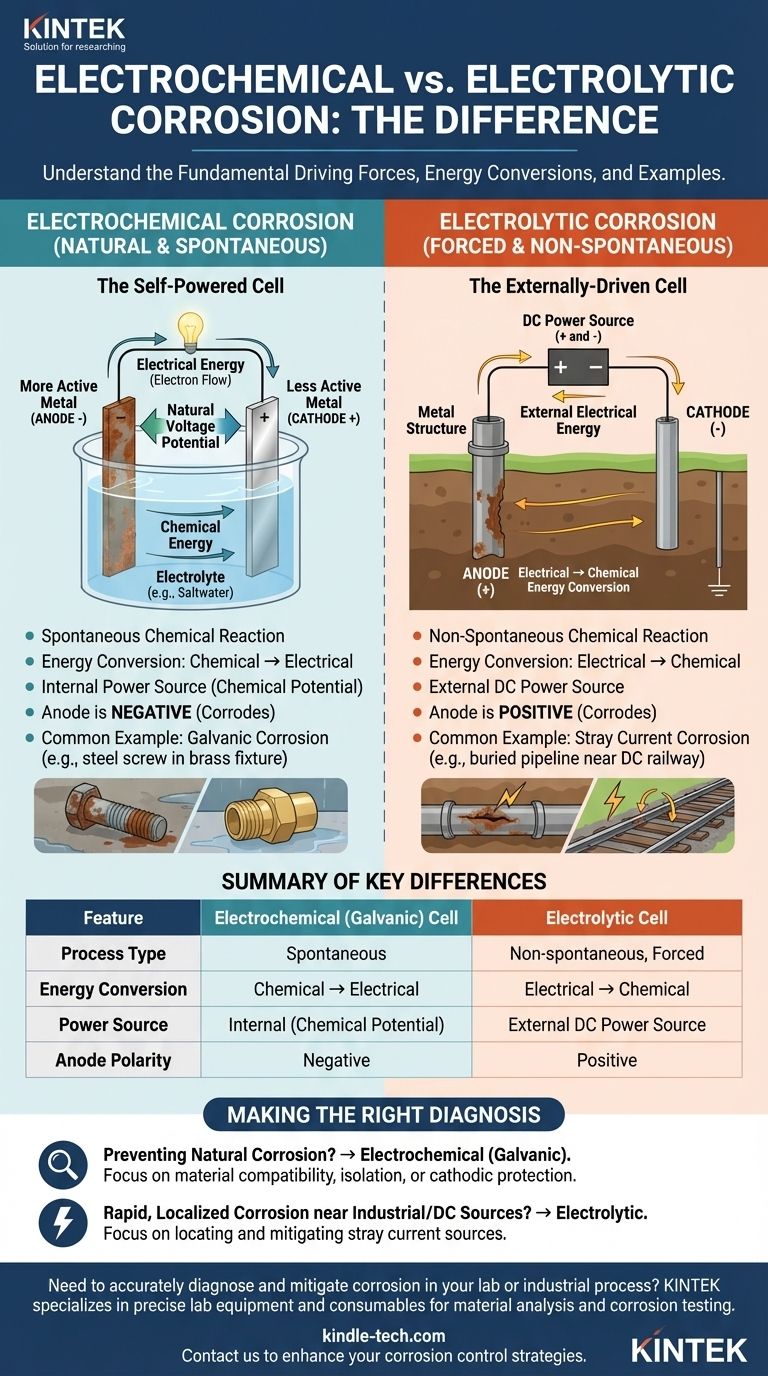
根本的なレベルでは、電解セルと電気化学的腐食セルの違いは、エネルギー変換と駆動力にあります。電気化学セルは、貯蔵された化学エネルギーを電気エネルギーに変換し、自然な腐食を引き起こす自発的なプロセスです。対照的に、電解セルは、外部の電気エネルギーを使用して化学反応を強制し、誘発された腐食を引き起こす非自発的なプロセスです。
核心的な区別は自発性です。電気化学的腐食は、バッテリーの放電のように自然に起こります。電解腐食は、鉄道システムからの迷走直流電流のように、外部電源によって材料に強制されます。
電気化学セル:腐食の自然な状態
電気化学セルは、ガルバニ電池とも呼ばれ、最も一般的な腐食の背後にあるメカニズムです。これは自己完結型の自然発生的なプロセスです。
自発的な化学反応
このタイプのセルは、2つの異なる金属が電解質(塩水など)の存在下で電気的に接触したときに形成されます。それらの間に自然な電圧差が存在します。
化学的に活性な方の金属がアノード(負極)となり腐食し、電子を放出します。活性の低い方の金属がカソード(正極)となり、これらの電子を受け入れます。
エネルギー変換:化学から電気へ
駆動力は、活性な金属内に貯蔵されている化学エネルギーの放出です。この化学エネルギーは、アノードからカソードへの電子の流れという形で電気エネルギーに直接変換されます。このプロセスには外部電源は必要ありません。
古典的な例はガルバニ腐食であり、湿潤環境で鋼製ネジ(アノード)が真鍮製の器具(カソード)に接続されている場合に急速に錆びる現象です。

電解セル:力による腐食
電解セルは、通常は起こらない化学反応を駆動します。これは、外部電源を適用することによって行われます。
非自発的な化学反応
このプロセスは、関与する材料の自然な傾向を克服します。外部電源は、金属がそうでなければ安定している場合でも、金属をアノードにして腐食するように強制します。
腐食は、この外部から供給された直流(DC)電流が金属構造物から電解質に流出する場所で発生します。
エネルギー変換:電気から化学へ
ここでは、外部電源からの電気エネルギーが化学エネルギーに変換され、それが腐食反応として現れます。セルは動作するために電力を消費します。
一般的な実世界のシナリオは迷走電流腐食です。DC駆動の鉄道の近くを通る埋設パイプラインは、漏洩電流を拾い、電流が土壌に戻って流出するパイプラインの部分を急速な速度で腐食させる可能性があります。
主な違いの理解
どちらのプロセスもアノード、カソード、電解質を伴いますが、それらの根本的な特性は反対です。これらの違いを認識することは、適切な診断と軽減のために不可欠です。
駆動力と電源
最も重要な区別は駆動力です。電気化学セルは、材料間の化学ポテンシャル差によって自己給電されます。電解セルは、外部DC電源によって外部給電されます。
電極の極性
両方のセル間でアノードとカソードの極性が反転しており、これはしばしば混乱の種となります。
- 電気化学(ガルバニ)セルでは、アノード(腐食が発生する場所)は負であり、カソードは正です。
- 電解セルでは、外部電源によりアノード(腐食が発生する場所)は正になり、カソードは負になります。
実際的な意味合い
腐食セルの種類を誤認すると、不適切な解決策につながります。たとえば、材料の組み合わせを変更することでガルバニ腐食の問題は解決するかもしれませんが、迷走電流腐食を止めることには何の効果もありません。
適切な診断を下す
根本的なメカニズムを理解することが、効果的な腐食制御への第一歩です。診断アプローチは、疑われるセルタイプによって導かれるべきです。
- 自然腐食の防止に主な焦点を当てる場合: おそらく電気化学的(ガルバニ)セルを扱っています。解決策には、適合する材料の選択、それらの電気的絶縁、または陰極防食の適用が含まれます。
- 産業設備やDC輸送機関の近くで急速な局所腐食を調査している場合: ほぼ間違いなく電解セルを扱っています。優先事項は、外部迷走電流の発生源を見つけて軽減することでなければなりません。
結局のところ、腐食が自然に発生しているのか、それとも外部の影響によって強制されているのかを知ることが、あなたの予防および制御戦略全体を決定します。
要約表:
| 特徴 | 電気化学(ガルバニ)セル | 電解セル |
|---|---|---|
| プロセスタイプ | 自発的 | 非自発的、強制 |
| エネルギー変換 | 化学 → 電気 | 電気 → 化学 |
| 電源 | 内部(化学ポテンシャル) | 外部DC電源 |
| アノード極性 | 負 | 正 |
| 一般的な例 | ガルバニ腐食(例:鋼/真鍮) | 迷走電流腐食(例:鉄道からのもの) |
研究室または産業プロセスにおける腐食の正確な診断と軽減が必要ですか?
腐食セルの正確なタイプを理解することが、効果的な解決策への第一歩です。KINTEKの専門家は、材料分析と腐食試験に必要な正確なラボ機器と消耗品を提供することを専門としています。ガルバニ反応の調査であれ、迷走電流効果の調査であれ、当社のツールはあなたの研究をサポートし、材料の完全性を確保します。
特定の研究室のニーズについて話し合い、KINTEKのソリューションが腐食制御戦略をどのように強化できるかを知るために、今すぐお問い合わせフォームからお問い合わせください。
ビジュアルガイド