専門的には、電気分解セルは特定の種類の電気化学セルです。この広いカテゴリーに属しますが、「電気化学セル」という用語は、まったく反対の機能を持つ別の装置であるガルバニ電池も指すことを理解することが重要です。
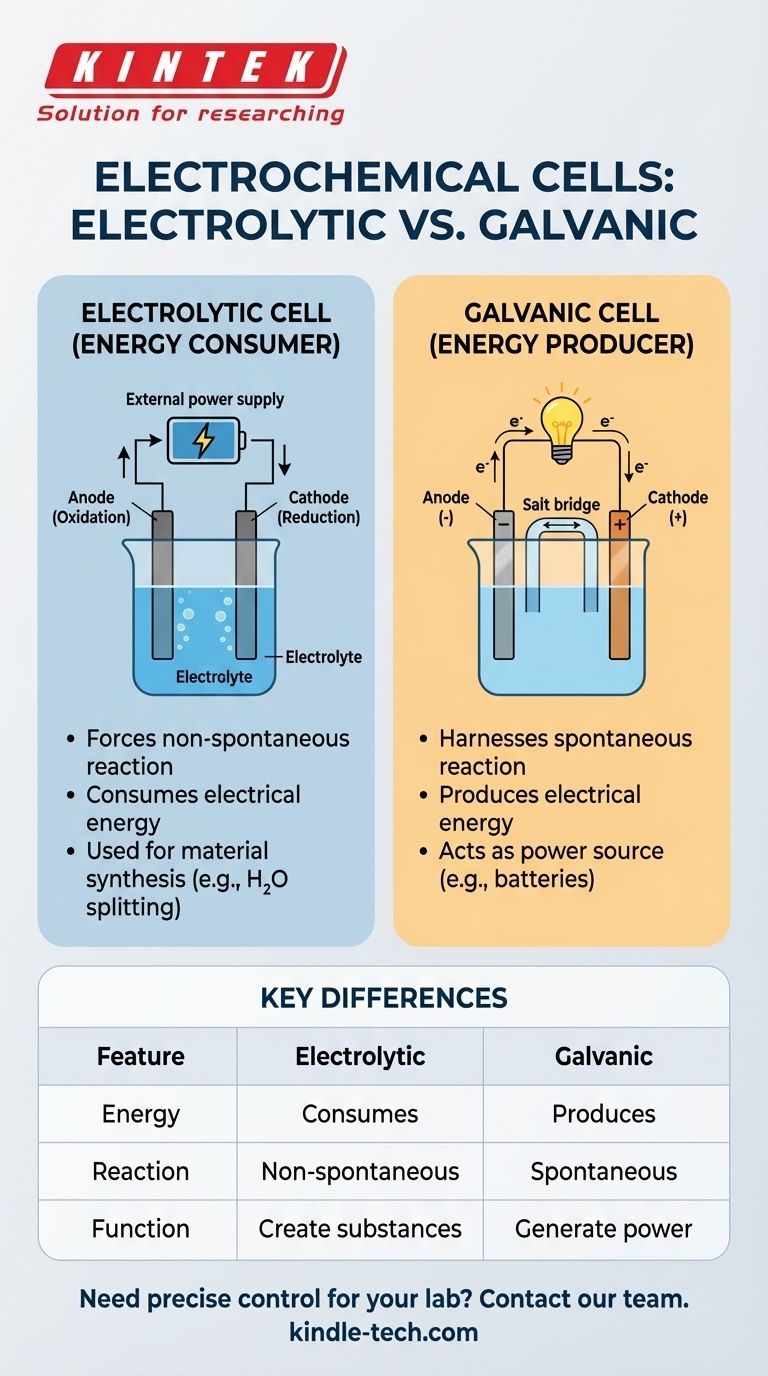
決定的な違いはこれです。電気分解セルは、外部の電気エネルギーを使用して、自発的には起こらない化学反応を強制的に引き起こします。これは電力を消費します。対照的に、ガルバニ電池(電池など)は、自発的な化学反応を利用して電気エネルギーを生成します。
中核機能:化学反応の強制
電気分解とは?
電気分解とは、直流(DC)電流を使用して、それ以外では非自発的な化学反応を駆動するプロセスです。簡単に言えば、電気を使って化学変化を起こさせることです。
このプロセスが発生する装置が電気分解セルまたは電解セルです。
外部電源の役割
電解セルの決定的な特徴は、バッテリーや電源などの外部電源を必要とすることです。この外部電圧は反応の自然なエネルギー障壁を克服し、化学物質に反応を強制します。
主要な構成要素
電解セルは、アノードとカソードの2つの電極で構成され、これらは電解質と呼ばれる液体溶液に浸されています。外部電源はアノードから電子を引き抜き(酸化)、カソードに電子を押し込み(還元)、目的の化学変化を駆動します。

電気分解セル vs. ガルバニ電池:「電気化学セル」という包括的な用語
電気化学セルという用語は、化学エネルギーと電気エネルギーを相互に変換するあらゆる装置の親カテゴリーです。明確にするためには、2つの主要なタイプを理解することが不可欠です。
電気分解セル:エネルギー消費者
これらのセルは、電気エネルギーを消費して化学変化を生成します。それらの主な目的は、強制的な反応を通じて物質を生成したり、材料を改変したりすることです。
一般的な例は、電気分解セルを使用して水をH₂Oから水素と酸素ガスに分解することですが、これにはかなりのエネルギー入力が必要です。
ガルバニ(ボルタ)セル:エネルギー生成者
これらのセルはその逆を行います。それらは自発的な化学反応を利用して電流を生成します。これがすべての一般的な電池の基本原理です。
電池を使用するとき、あなたはガルバニセルを利用して、蓄えられた化学エネルギーを使用可能な電力に変換しています。
区別が重要な理由
電気分解セルを「電気化学セル」と呼ぶのは技術的には正しいですが、不正確です。それは、正方形を「長方形」と呼ぶようなものです。真実ではありますが、それを定義する特定の特性が省略されます。主な違いは常にエネルギー変換の方向です。
一般的な用途とトレードオフ
電気分解が使用される場所
化学反応を強制する能力は、産業的に計り知れない価値があります。電気分解セルは、燃料用の純粋な水素の生産、鉱石からのアルミニウムや銅などの金属の精錬、物体へのクロムや金などの薄い金属層の電気めっきに不可欠です。
主なトレードオフ:エネルギーコスト
電気分解の主な制限は、高いエネルギー消費です。非自発的な反応を強制するため、このプロセスは常に、蓄積する化学エネルギーや生成物の価値よりも多くのエネルギーを必要とします。このエネルギーコストは、あらゆる産業用電気分解プロセスの中心的な経済的および環境的考慮事項です。
目標に合った適切なセルの特定方法
- エネルギーの貯蔵または材料(水素燃料や純粋なアルミニウムなど)の生成が主な焦点である場合: 化学反応を駆動するために電力を消費する電気分解セルを扱っています。
- 化学源からの電力生成(電池など)が主な焦点である場合: 自発的な反応から電力を生成するガルバニ(またはボルタ)セルを扱っています。
- 両方のプロセスを網羅する一般的な科学分野が主な焦点である場合: 包括的な用語である電気化学セルを使用する必要があります。
結局のところ、エネルギーの流れの方向、つまりエネルギーが消費されているのか生成されているのかを理解することが、これらの基本的な装置を区別する鍵となります。
要約表:
| 特徴 | 電気分解セル | ガルバニセル |
|---|---|---|
| エネルギー変換 | 電気エネルギーを消費する | 電気エネルギーを生成する |
| 反応タイプ | 非自発的(強制) | 自発的 |
| 主な機能 | 物質の生成(例:H₂、精錬された金属) | 電力の生成(例:電池) |
| 電源 | 外部電源が必要(例:電池、電源) | それ自体が電源である |
実験室で化学反応を正確に制御する必要がありますか?
材料合成、電気めっき、エネルギー貯蔵など、あなたの研究が何であれ、適切な機器を所有することが不可欠です。KINTEKは、信頼性と精度のために設計された電気化学セルや電源を含む、高品質の実験室機器と消耗品を専門としています。
当社の専門家が、特定の用途に最適なセットアップの選択をお手伝いします。今すぐ当社のチームに連絡して、実験室のニーズについてご相談いただき、KINTEKがお客様の研究目標をどのようにサポートできるかをご確認ください。
ビジュアルガイド
関連製品
- 多様な研究用途に対応するカスタマイズ可能なPEM電解セル
- 薄層分光電気分解セル
- 電解電気化学セル ガス拡散液体フロー反応セル
- 電気化学実験用石英電解電気化学セル
- PTFE電解セル 電気化学セル 耐腐食性 シール・非シール



















