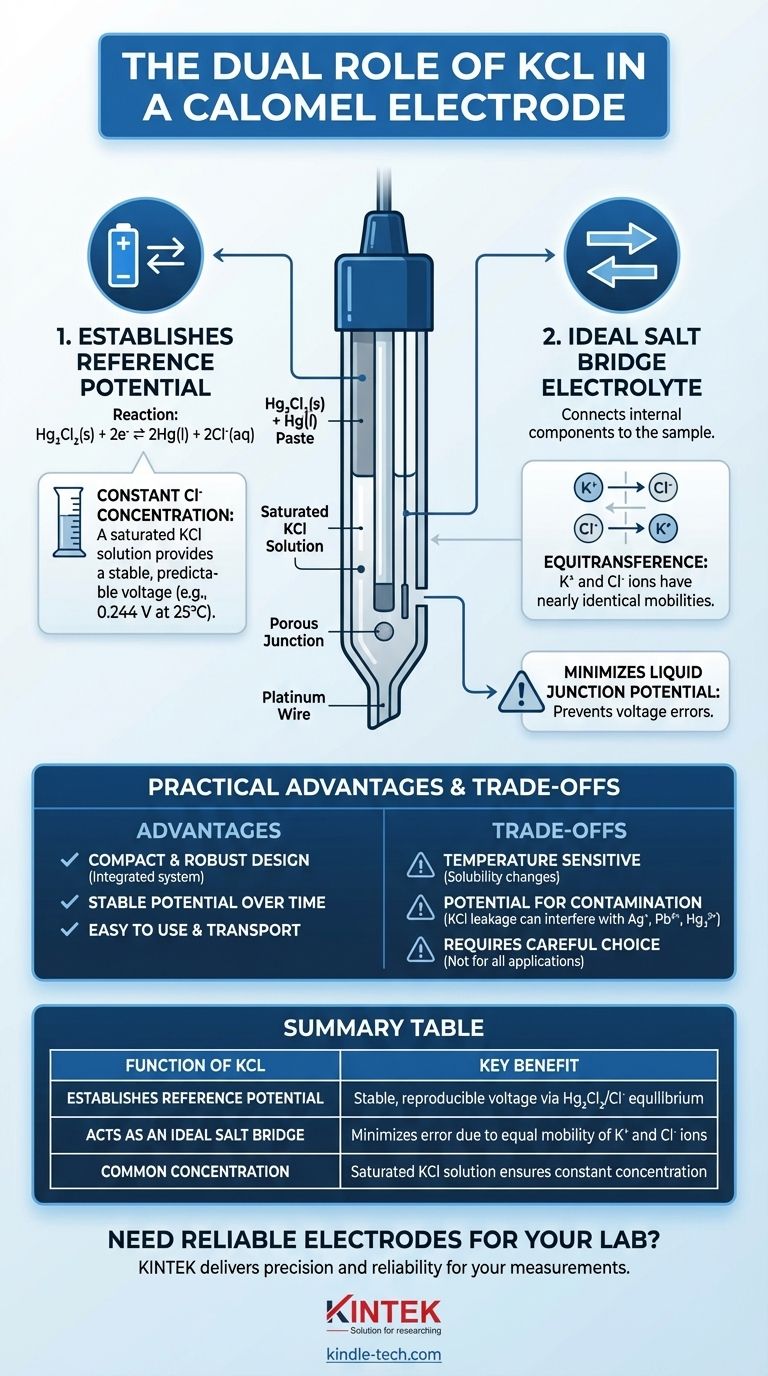
本質的に、塩化カリウム(KCl)がカロメル電極に使用されるのは、2つの重要な理由からです。 第一に、塩化物イオン(Cl⁻)は、電極の安定した電圧を確立する化学反応の主要な構成要素です。第二に、そのカリウム(K⁺)イオンと塩化物(Cl⁻)イオンは、溶液中をほぼ同じ速度で移動します。これは、理想的な塩橋電解質の決定的な特徴です。
KClの二重機能がカロメル電極の成功の鍵です。それは単なる受動的な構成要素ではなく、参照電位の設定に積極的に関与すると同時に、非常に効果的な塩橋として機能することで測定誤差を防ぎます。
電極機能におけるKClの二重の役割
KClの選択は、安定した、再現性のある、便利な参照電極を作成するために意図的に行われた工学的な選択です。それは、2つの異なるが等しく重要な目的を果たします。
参照電位の確立
カロメル電極の電圧は、特定の化学平衡によって生成されます: Hg₂Cl₂(s) + 2e⁻ ⇌ 2Hg(l) + 2Cl⁻(aq)。
この反応の電位は、溶液中の塩化物イオン(Cl⁻)の濃度に直接依存します。既知の一定濃度のKCl溶液で電極を満たすことにより、安定した予測可能な参照電位が確立されます。
最も一般的には、飽和KCl溶液が使用されます。これにより、たとえ水分が蒸発しても濃度が一定に保たれ、再現性の高い電圧が得られるため、電気化学測定の信頼できる基準となります。
理想的な塩橋としての機能
KCl溶液は、参照電極の内部コンポーネントを測定対象のサンプル溶液に接続する塩橋としても機能します。
効果的な塩橋には、その陽イオンと陰イオンが溶液中をほぼ同じ速度で移動することが必要です。この特性は等電移動性(equitransference)として知られています。
もし一方のイオンが他方よりも著しく速く移動すると、2つの溶液間の境界で電荷分離が生じます。これにより、液間電位として知られる望ましくない電圧が発生し、測定に重大な誤差を導入します。
K⁺イオンとCl⁻イオンの移動度はほぼ同じであるため、この液間電位が最小限に抑えられ、測定の精度が保証されます。

実用的な利点とトレードオフ
KClの使用は大きな実用的な利点をもたらしますが、すべての分析者が理解しなければならない考慮事項も導入します。
KClが便利な理由
KClの統合された性質—電極反応と塩橋の両方に役立つ—は、コンパクトで堅牢な設計を可能にします。
カロメル電極は、別個の外部塩橋を必要としません。これにより、他の参照システムと比較して、セットアップ、使用、および輸送が容易になります。その電位は、時間の経過とともに非常に安定していることも知られています。
濃度の影響
カロメル電極の電位は、KCl濃度に完全に依存します。飽和KClが最も一般的ですが、1 Mや0.1 Mなどの他の濃度も特定の用途で使用されます。
飽和溶液を使用することは、濃度が自己調整されるため便利ですが、KClの溶解度が温度によって変化するため、電極の電位が温度変化に敏感になることも意味します。
汚染の可能性
重要なトレードオフは、電極の充填溶液が多孔質接合部を介してサンプルにゆっくりと漏れ出す可能性があることです。
分析に、塩化物と沈殿するイオン(銀(Ag⁺)、鉛(Pb²⁺)、水銀(Hg₂²⁺)など)が含まれる場合、漏れ出したKClが干渉を引き起こし、不正確な結果を招く可能性があります。
目標に合った適切な選択をする
KClの役割を理解することで、カロメル電極が特定の電気化学測定に適したツールであるかどうかを判断するのに役立ちます。
- 再現性と使いやすさを最優先する場合: 飽和カロメル電極(SCE)は、サンプルに干渉イオンがなく、温度が安定している限り、優れた古典的な選択肢です。
- 塩化物汚染を最小限に抑えることを最優先する場合: 塩化物を含まない電解質を使用する水銀-硫酸第一水銀電極など、別の参照システムを使用する必要があります。
- 様々な温度での性能を最優先する場合: 非飽和KCl溶液(例:3 M)を使用する電極は、飽和バージョンよりも温度変化に対する電位が安定しています。
最終的に、KClの選択はカロメル電極の設計の基本であり、正確で信頼性の高い測定に必要な安定した基盤を提供します。
要約表:
| KClの機能 | 主な利点 |
|---|---|
| 参照電位を確立する | Hg₂Cl₂/Cl⁻平衡を介して安定した再現性のある電圧を提供する。 |
| 理想的な塩橋として機能する | K⁺イオンとCl⁻イオンの移動度がほぼ等しいため、測定誤差を最小限に抑える。 |
| 一般的な濃度 | 飽和KCl溶液は濃度を一定に保ち、再現性を高める。 |
研究室の電気化学分析に信頼性の高い参照電極が必要ですか?
KINTEKでは、お客様の測定精度が質の高い実験機器に依存していることを理解しています。当社の電極と消耗品のラインナップは、お客様の研究室が必要とする精度と信頼性を提供するように設計されています。
当社の専門家が、お客様の特定の用途に最適な機器の選択をお手伝いします。今すぐKINTEKにお問い合わせください。お客様のニーズについて話し合い、研究室の成功を確実にしましょう!
ビジュアルガイド