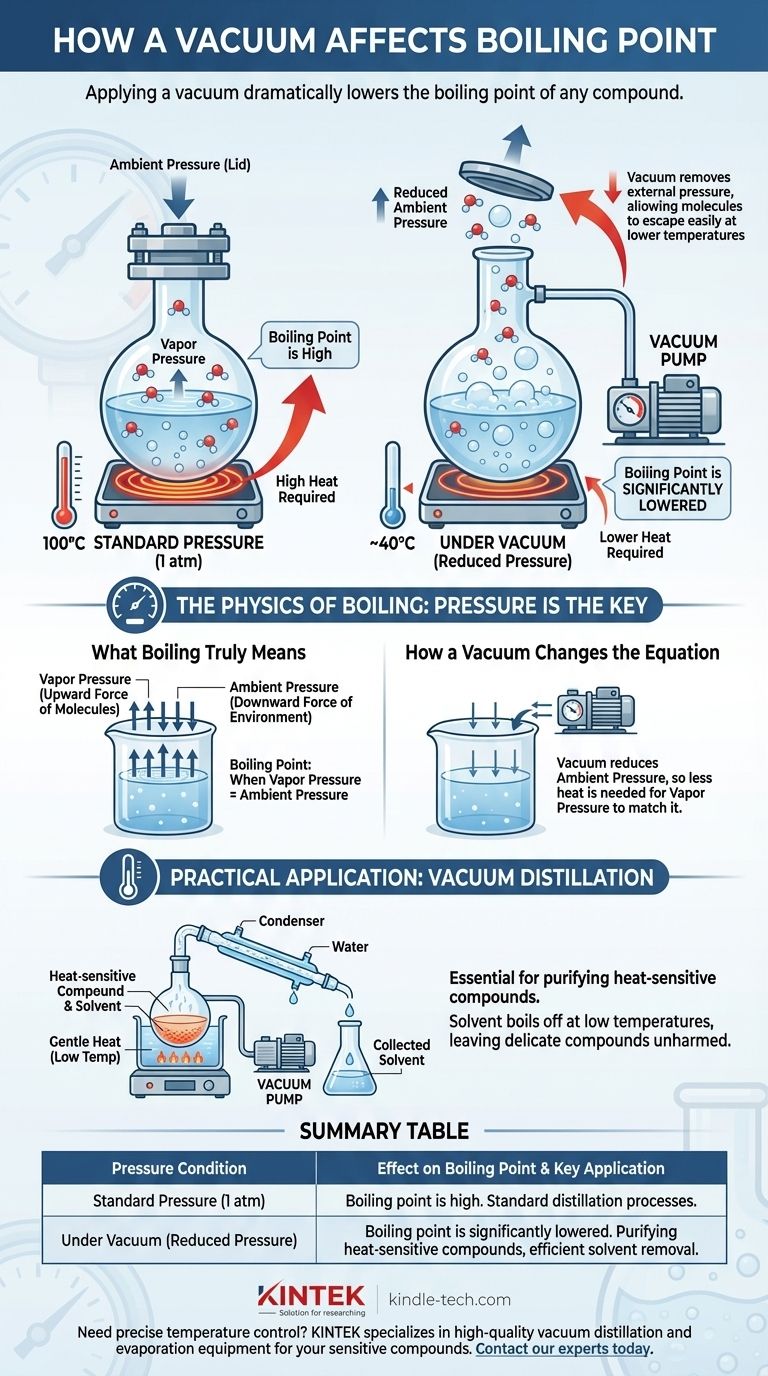
要するに、真空を適用すると、あらゆる化合物の沸点が劇的に低下します。 沸騰は固定された温度ではなく、液体の内部蒸気圧がその表面に押しかかる外部圧力と等しくなる点です。真空を作り出すことで、その外部圧力を取り除き、分子がはるかに低い温度で液体相から逃げて気体になるのをずっと容易にします。
液体の沸点は一定ではありません。それは周囲の圧力の直接的な関数です。真空によってこの圧力を下げることは、分子が気体に相変化するために必要なエネルギーを低下させ、物質が大幅に低い温度で沸騰するようにします。
沸騰の物理学:圧力が鍵
真空がなぜそれほど強力な効果を持つのかを理解するためには、まず「沸騰」が実際には何であるかを再定義する必要があります。それは特定の温度というよりも、圧力の戦いなのです。
沸騰が真に意味するもの
沸騰とは、液体の蒸気圧がその環境の大気圧と等しくなる特定の物理状態です。
この平衡点に達すると、蒸気の泡が液体の内部で形成され、表面に上昇することができます。これは、液体の表面でのみ起こる単純な蒸発とは根本的に異なります。
蒸気圧の役割
すべての液体は一定の蒸気圧を発生させます。これは、分子が気相に逃れようとする固有の力です。
液体を加熱すると、分子は運動エネルギーを得ます。このエネルギーの増加により、周囲に対してより強く押し付けられるようになり、したがって、蒸気圧は温度とともに増加します。
大気圧が「蓋」として機能する方法
私たちの周りの大気は、液体表面を含むすべてに一定の圧力をかけています。この大気圧を、液体の分子を所定の位置に保持する物理的な「蓋」と考えることができます。
液体が沸騰するためには、その蒸気圧が「蓋を押し上げる」のに十分な強さになる必要があります。海抜(1気圧)では、水を沸騰させるには、水が212°F(100°C)に達して、これを達成するのに十分な蒸気圧を発生させる必要があります。

真空が方程式をどのように変えるか
真空ポンプは、密閉されたシステムからガス分子を除去することにより、大気圧を劇的に低下させます。これは沸騰に必要な条件を根本的に変えます。
「蓋」の除去
真空を適用することは、その圧力の「蓋」を持ち上げることと同等です。液体の表面に押し下げるガス分子が少なくなるため、分子ははるかに容易に逃げることができます。
これは、高地で水がより低い温度で沸騰するのと同じ理由です。山の上では大気圧が低いため、水の蒸気圧がそれに一致するために必要な熱が少なくて済みます。
新しい、より低い沸点
外部圧力がはるかに低くなったため、液体は蒸気圧を沸点まで高めるためにより多くの熱エネルギーを必要としません。
その結果、物質は標準沸点よりもはるかに低い温度で沸騰します。たとえば、十分な真空下では、水を室温で沸騰させることができます。
実用的な応用:減圧蒸留
この原理は、熱に弱い化合物を精製するために化学において不可欠です。化学者は混合物を真空下に置き、穏やかに加熱することができます。
揮発性の溶媒は非常に低い温度で沸騰して除去され、熱に敏感な望ましい化合物は、潜在的に損傷を与える可能性のある高温にさらされることなく残されます。
トレードオフと落とし穴の理解
沸点を下げるために真空を使用することは強力ですが、課題がないわけではなく、慎重な検討が必要です。
「突沸」のリスク
真空下では、液体は突沸と呼ばれる現象で爆発的に沸騰することがあります。不均一な加熱は、液体の特定の部分が過熱し、激しい力で突然蒸気に変わる原因となる可能性があります。これは通常、沸騰石の使用または絶え間ない撹拌によって管理されます。
低揮発性物質の難しさ
非常に弱い分子間力、したがって非常に低い蒸気圧を持つ物質(油やイオン液体など)の場合、たとえ高真空であっても、熱分解を防ぐのに十分なほど沸点を下げられないことがあります。この技術の有用性には実用的な限界があります。
機器とシールの完全性
深い真空を達成し維持するには、特殊なポンプと完全に密閉されたガラス器具または容器が必要です。わずかな漏れでもシステムの圧力を損ない、沸点が予期せず上昇する可能性があります。
目的のための適切な選択
圧力の操作はツールであり、その適用は完全にあなたの目的に依存します。
- 熱に弱い化合物の精製が主な目的の場合: 減圧蒸留を使用して、分解や望ましくない副反応を防ぐ温度で成分を分離します。
- 溶媒を効率的に除去することが主な目的の場合: 高熱を必要とせずに溶媒を急速に蒸発させるために、真空(多くの場合回転を伴う、回転蒸発器など)を適用します。
- デリケートな材料を脱水することが主な目的の場合: 深い真空を使用して水の沸点/昇華点を下げ、材料の構造を維持する低温での脱水(フリーズドライ)を可能にします。
結局のところ、圧力と温度の関係を理解することは、物質の物理的状態を正確に制御することを可能にします。
要約表:
| 圧力条件 | 沸点への影響 | 主な用途 |
|---|---|---|
| 標準圧力(1気圧) | 沸点は標準の高温になります。 | 標準的な蒸留プロセス。 |
| 真空下(減圧) | 沸点が大幅に低下します。 | 熱に弱い化合物の精製、効率的な溶媒除去。 |
デリケートな化合物に正確な温度制御が必要ですか? KINTEKは、沸点を下げることでデリケートな材料を保護するために設計されたロータリーエバポレーターを含む、高品質の減圧蒸留および蒸発装置を専門としています。当社の実験装置は、研究者や実験室の専門家のために効率的で安全な処理を保証します。当社の専門家に今すぐお問い合わせいただき、お客様の用途に最適な真空ソリューションを見つけてください!
ビジュアルガイド