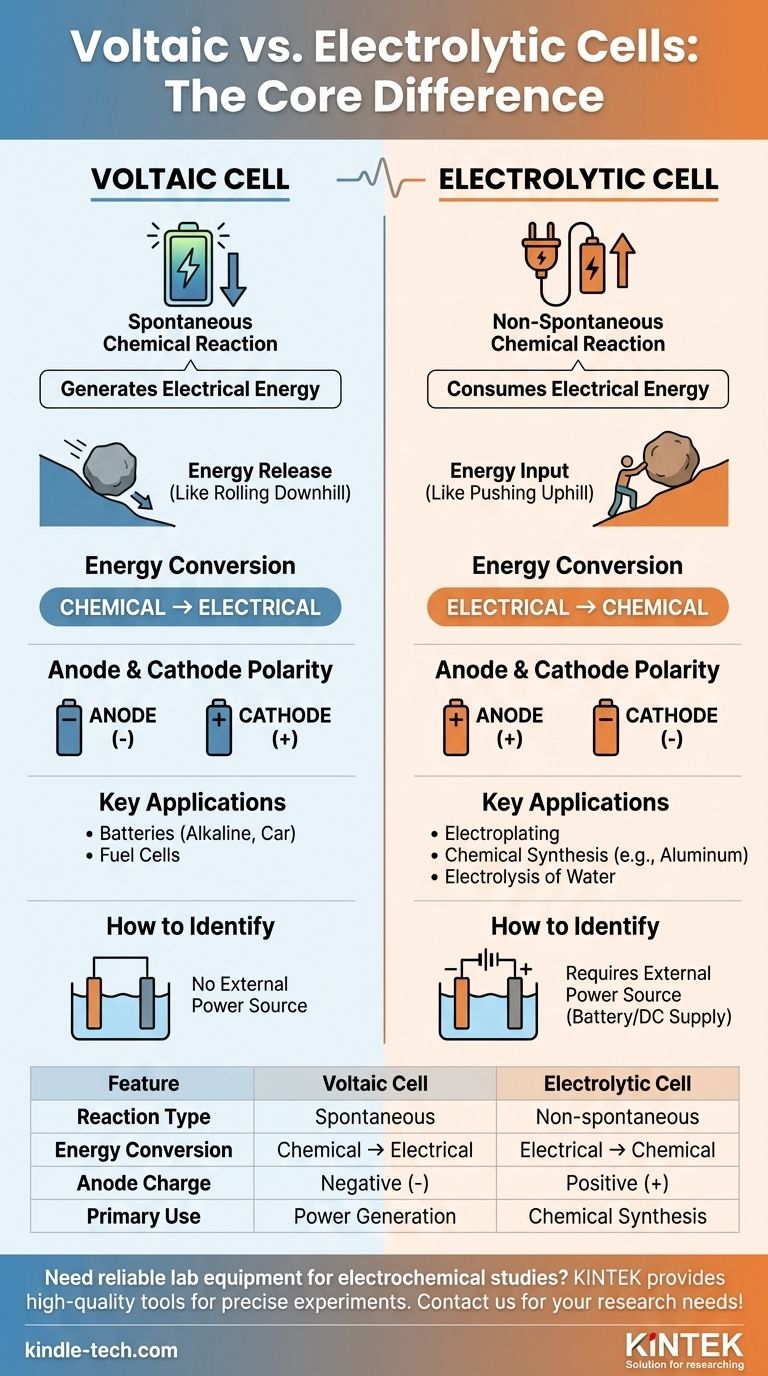
ボルタ電池と電解槽の主な違いは、その根本的な目的と関与する化学反応の性質にあります。一般的な電池のようなボルタ電池は、自発的な化学反応を利用して電気エネルギーを生成します。対照的に、電解槽は外部の電気エネルギーを利用して、それ自体では起こらない化学反応を駆動します。
その核心において、この区別はエネルギーの流れに関するものです。ボルタ電池は、自発的な化学反応からエネルギーを放出する電源です。電解槽は、自発的ではない化学反応を強制的に起こさせるエネルギー消費者です。
核心原理:自発性
これら2つの電池を区別する最も重要な概念は、化学反応が自発的であるか非自発的であるかです。これが電池全体の機能と構造を決定します。
ボルタ電池:自発的なエネルギー放出
ボルタ電池(ガルバニ電池とも呼ばれる)では、酸化還元反応は自発的です。反応物は生成物よりも高い化学ポテンシャルエネルギーを持っています。
この自然な反応傾向がエネルギーを放出し、それが電流として利用されます。これは、岩が坂を転がり落ちるようなもので、外部からの押し出しなしに起こります。
ボルタ電池の標準電池電位(E°cell)は常に正であり、自発的な反応を示します。
電解槽:強制的な化学変化
電解槽では、酸化還元反応は非自発的です。生成物は反応物よりも高いエネルギー状態にあります。
この反応を起こさせるためには、外部電源(電池や直流電源など)を印加する必要があります。これは、岩を坂の上へ押し上げるようなもので、絶え間ないエネルギーの入力が必要です。
電解槽内の反応の標準電池電位(E°cell)は負であり、外部からの助けなしには進行しないことを示しています。

主な機能的および構造的違い
自発性の違いは、これらの電池がどのように構築され、どのように動作するかにおいて、いくつかの重要な区別をもたらします。
エネルギー変換
ボルタ電池は、化学エネルギーを電気エネルギーに変換します。これは化学的な発電機です。
電解槽は、その逆を行います。電気エネルギーを化学エネルギーに変換し、電力を使って新しい物質を生成します。
アノードとカソードの極性
これは頻繁に混乱する点ですが、核となる定義を覚えていれば簡単です。どちらの電池タイプでも、酸化は常にアノードで起こり、還元は常にカソードで起こります。
ただし、これらの電極の電荷は逆になります。
- ボルタ電池では、アノードは自発的な反応からの電子源であるため、負極 (-) となります。カソードは電子が消費される場所であるため、正極 (+) となります。
- 電解槽では、外部電源が電荷を決定します。外部電源は電子をカソードに押し込むため、カソードは負極 (-) となります。アノードから電子を引き離すため、アノードは正極 (+) となります。
実用的な応用
各電池タイプの応用は、その機能に直接反映されます。
ボルタ電池は、デバイスの電力供給に使用されます。例としては、日常のアルカリ電池、自動車のバッテリー(放電中)、燃料電池などがあります。
電解槽は、合成と精製に使用されます。一般的な応用としては、金属の電気めっき、純粋なアルミニウムの製造、水電解による水素ガスと酸素ガスの生成などがあります。
よくある落とし穴と重要な区別
よくある間違いを避けるためには、電池の目的と外部電源の有無に焦点を当ててください。
目的:電力 vs. 生産
これらを区別する最も簡単な方法は、その目標によるものです。電池は電気を生成しているのか、それとも電気を使って化学物質を生成しているのか?前者はボルタ電池、後者は電解槽です。
塩橋の役割
ボルタ電池は、しばしば塩橋で接続された2つの別々の半電池で構成されます。この構成要素は、自発的な反応中にイオンが流れる際に電荷中性を維持するために不可欠です。
電解槽は通常、より単純な構造をしており、電解質自体がイオン移動を可能にする単一の容器内で反応が起こることが多いです。
外部電源
図における最も明確な視覚的指標は、電池または電源の存在です。電極に接続されているものが見える場合、それは電解槽です。その不在はボルタ電池を示唆します。
目的に合った選択をする
電池の種類を特定したり、その機能を理解したりするには、システムの主要な目的を考慮してください。
- デバイスに電力を供給することが主な目的の場合: 自発的な化学反応を利用して電流を生成するボルタ電池を扱っています。
- 純粋な物質(塩素ガスや銅金属など)を生成することが主な目的の場合: 外部電源で非自発的な反応を駆動する電解槽を使用しています。
- 外部バッテリーが接続された図を分析している場合: これは電解槽を示しており、化学変化を強制するために必要なエネルギーを供給しています。
自発的な生成と強制的な反応というこの根本的な区別を理解することが、電気化学をマスターする鍵となります。
要約表:
| 特徴 | ボルタ電池 | 電解槽 |
|---|---|---|
| 反応タイプ | 自発的 | 非自発的(外部電源が必要) |
| エネルギー変換 | 化学 → 電気 | 電気 → 化学 |
| アノードの電荷 | 負 (-) | 正 (+) |
| 主な用途 | 発電(例:電池) | 化学合成(例:電気めっき) |
電気化学研究のための信頼性の高い実験装置が必要ですか? KINTEKは高品質の実験装置と消耗品を専門としており、ボルタ電池や電解槽を伴う実験に必要な精密なツールを提供しています。電極から電源まで、当社のソリューションは、お客様の実験室で正確で再現性のある結果を保証するのに役立ちます。今すぐお問い合わせください お客様の研究ニーズに最適な機器を見つけるために!
ビジュアルガイド